Белки – это ВМС (биополимеры), структурную основу которых составляют полипептидные цепи, построенные из остатков α-аминокислот.
Физические свойства белков
Свойства белков также разнообразны, как и их функции. Одни белки растворяются в воде и образуют коллоидные растворы (например, яичный белок); другие растворимы в разбавленных растворах солей; третьи вообще нерастворимы (например, белки покровных тканей).
Химические свойства белков
В радикалах аминокислотных остатков белки содержат различные функциональные группы, способные вступать во многие реакции: окисления-восстановления, алкилирования, этерификации, нитрирования. Белки могут образовывать соли как с кислотами, так и с основаниями (белки амфотерны).
Функции белков в организме
Белки выполняют в организмах множество функций
| Пластическая | Строительный материал клеток | Например, коллаген, мембранные белки |
| Транспортная | Переносят различные вещества | Например, гемоглобин (перенос кислорода и углекислого газа) |
| Защитная | Обезвреживают чужеродные вещества | Например, γ-глобулин, сыворотка крови |
| Энергетическая | Снабжают организм энергией | При расщеплении 1гр. белка освобождается 17,6 кДж энергии |
| Сократительная | Выполняет все виды движений, к которым способны клетки организма | Например, миозин (белок мышц) |
| Регуляторная | Регулируют обменные процессы | Гормоны, например, инсулин (обмен глюкозы) |
| Каталитическая | Ускоряют протекание химических реакций в организме | По своей химической природе все ферменты являются белками. Например, рибонуклеаза |
Нуклеиновые кислоты
Нуклеиновые кислоты – природные ВМС, макромолекулы которых состоят из мононуклеотидов.
Нуклеиновые кислоты бывают двух типов:
Полисахариды
Полисахариды – высокомолекулярные углеводороды, образованные остатками моносахаридов (глюкозы, фруктозы) или их производных (аминосахаров). Образуют в биосфере основную массу органического вещества.
Из высших полисахаридов наибольшее значение имеют клетчатка (или целлюлоза), крахмал и гликоген (животный крахмал).
Целлюлоза содержится в стеблях растений, в древесине и коре деревьев. Хлопок содержит порядка 90% целлюлозы, хвойные породы деревьев – свыше 60%, лиственные – 40%. Целлюлоза также составляет структурную основу некоторых бактерий.
Крахмал выполняет роль резервного пищевого вещества в растениях. Плоды, клубни, семена могут содержать до 70% крахмала. Гликоген (запасаемый полисахарид животных) содержится главным образом в печени и мышцах.
Полисахариды присутствуют во всех живых организмах, выполняют функции защитных (слизь, камедь) и запасных (гликоген, крахмал) веществ. Обеспечивают сцепление клеток в тканях животных и растений. Участвуют в иммунных реакциях.
Природные полимеры образуются в клетках живых организмов в процессе биосинтеза. С помощью фракционного осаждения, экстракции и других методов они могут быть выделены из животного и растительного сырья.
По материалам «Химия. Пособие-репетитор для поступающих в вузы // 6-е изд. – Ростов н/Д: 2003.» под ред. А.С.Егорова
Биополимеры , высокомолекулярные природные соединения, являющиеся структурной, основой всех живых организмов и играющие определяющую роль в процессах жизнедеятельности. К Биополимеры относятся белки, нуклеиновые кислоты и полисахариды; известны также смешанные Биополимеры - гликопротеиды, липопротеиды, гликолипиды и др.Биологические функции Биополимеры Нуклеиновые кислоты выполняют в клетке генетические функции. Последовательность мономерных звеньев (нуклеотидов) в дезоксирибонуклеиновой кислоте - ДНК (иногда в рибонуклеиновой кислоте - РНК) определяет (в форме генетического кода ) последовательность мономерных звеньев (аминокислотных остатков) во всех синтезируемых белках и, т. о., строение организма и протекающие в нём биохимические процессы. При делении каждой клетки обе дочерние клетки получают полный набор генов благодаря предшествующему самоудвоению (репликации ) молекул ДНК. Генетическая информация с ДНК переносится на РНК, синтезируемую на ДНК как на матрице (транскрипция ). Эта т. н. информационная РНК (и-РНК) служит матрицей при синтезе белка, происходящем на особых органоидах клетки - рибосомах (трансляция ) при участии транспортной РНК (т-РНК). Биологическая изменчивость, необходимая для эволюции, осуществляется на молекулярном уровне за счёт изменений в ДНК (см. Мутация ).
Статья про слово "Биополимеры " в Большой Советской Энциклопедии была прочитана 11115 раз
Состав белков. Белки - обязательная составная часть всех клеток . В состав этих биополимеров входят мономеры 20 типов. Такими мономерами являются аминокислоты, которые состоят из атомов углерода, водорода, кислорода, азота и серы.
В результате соединения аминокислот однотипной химической связью, образуются линейные молекулы белков. В составе большинства белков находится в среднем 300-500 остатков аминокислот. Известно несколько очень коротких природных белков, длиной в 3-8 аминокислот, и очень длинных биополимеров, длиной более чем в 1500 аминокислот.
Каждая из 20 аминокислот отличается от любой другой аминокислоты особой химической группировкой, так называемой R-группой или радикалом.
Строение белков . Выделяют первичную, вторичную, третичную и четвертичную структуры белков .
Первичная структура определяется порядком чередования аминокислот в цепи. Двадцать разных аминокислот можно уподобить 20 буквам химического алфавита, из которых составлены «слова» длиной в 300-500 букв. С помощью 20 букв можно написать безграничное множество таких длинных слов. Если считать, что замена или перестановка хотя бы одной буквы в слове придает ему новый смысл, то число комбинаций в слове длиной в 500 букв составит 20500.
Известно, что замена даже одного аминокислотного звена другим в белковой молекуле изменяет ее свойства. В каждой клетке содержится несколько тысяч разных видов белковых молекул, и для каждого из них характерна строго определенная последовательность аминокислот. Именно порядок чередования аминокислот в данной белковой молекуле определяет ее особые физико-химические и биологические свойства. Исследователи умеют расшифровывать последовательность аминокислот в длинных белковых молекулах и синтезировать такие молекулы.
В живой клетке многие белки или отдельные участки их представляют собой не вытянутую нить, а спираль с одинаковыми расстояниями между витками. Такая спираль представляет собой вторичную структуру белковой молекулы.
Спираль обычно свернута в клубок. Этот клубок образован закономерным переплетением участков белковой цепи. Положительно и отрицательно заряженные группы аминокислот притягиваются и сближают даже далеко отстоящие друг от друга участки белковой цепи. Сближаются и иные участки белковой молекулы, несущие, например, «водоотталкивающие» (гидрофобные) группы. В результате взаимодействия различных остатков аминокислот спирализованная молекула белка образует клубок - третичную структуру. Для каждого вида белка характерна своя форма клубка с изгибами и петлями. Третичная структура зависит от первичной структуры, т. е. от порядка расположения аминокислот в цепи.
Наконец, некоторые белки, например гемоглобин, состоят из нескольких цепей, различающихся по первичной структуре. Объединяясь вместе, они создают сложный белок, обладающий не только третичной, но и четвертичной структурой.
Белки - строительные материалы. Некоторые бактерии и все растения способны синтезировать все аминокислоты, из которых строятся белки, используя для этого неорганические вещества: азот и углекислый газ воздуха, водород, полученный при расщеплении воды (за счет энергии света), неорганические вещества почвы. Животные в процессе эволюции утратили способность осуществлять синтез десяти особенно сложных аминокислот, называемых незаменимы. Они получают их в готовом виде с растительной и животной пищей. Такие аминокислоты содержатся в белках молочных продуктов (молоко, сыр, творог), в яйцах, рыбе, мясе, а также в сое, бобах и некоторых других растениях. В пищеварительном тракте белки расщепляются до аминокислот, которые всасываются в кровь и попадают в клетки. В клетках из готовых аминокислот строятся собственные белки, характерные для данного организма. Белки являются обязательным компонентом всех клеточных структур и в этом состоит их важная структурная роль.
Белки - ферменты. В каждой живой клетке происходят непрерывно сотни биохимических реакций. В ходе этих реакций идут расщепление и окисление поступающих извне питательных веществ. Полученную вследствие окисления энергию питательных веществ и продукты их расщепления клетка использует для синтеза необходимых ей разнообразных органических соединений. Быстрое протекание таких реакций обеспечивают биологические катализаторы, или ускорители реакций - ферменты. В настоящее время известно более тысячи ферментов. Каждый фермент обеспечивает одну реакцию или несколько реакций одного типа. Например, жиры в пищеварительном тракте (а также внутри клеток) расщепляются специальным ферментом, который не действует на полисахариды (крахмал, гликоген) или на белки. В свою очередь, фермент, расщепляющий только крахмал или гликоген, не действует на жиры. Каждая молекула фермента способна осуществлять от нескольких тысяч до нескольких миллионов операций в минуту. В ходе этих реакций ферментный белок не расходуется. Он соединяется с реагирующими веществами, ускоряет их превращения и выходит из реакции неизменным.
Ферменты выполняют работу наилучшим образом. Только при оптимальной температуре (например, у человека и теплокровных животных при 37° С). Для ферментативных реакций нужна определенная концентрация ионов водорода в среде.
Процесс расщепления или синтеза любого вещества в клетке, как правило, разделен на ряд химических операций. Каждую операцию выполняет отдельный фермент. Группа таких ферментов составляет своего рода биохимический конвейер.
Регуляторные белки. Известно, что в специализированных клетках животных и растений производятся специальные регуляторы физиологических процессов - гормоны. Часть гормонов (но не все) животных и человека являются белками. Так, белковый гормон (гормон поджелудочной железы) инсулин активирует захват клетками молекул глюкозы и расщепление или запасание их внутри клетки. Если не хватает инсулина, то глюкоза накапливается в крови в избытке. Клетки без помощи инсулина не способны ее захватить - они голодают. Именно в этом причина развития диабета - болезни, вызываемой недостатком инсулина в организме.
Гормоны выполняют важнейшую функцию в организме, управляя активностью ферментов. Так, инсулин активирует в клетках печени фермент, синтезирующий из глюкозы другое органическое вещество - гликоген и ряд других ферментов.
Белки - средства защиты. При попадании бактерий или вирусов в кровь животных и человека организм реагирует выработкой специальньгх защитных белков - антител. Эти белки связываются с чужеродными для организма белками возбудителей заболеваний, чем подавляется их жизнедеятельность. На каждый чужеродный белок организм вырабатывает специальные «антибелки» - антитела.
Антитела обладают удивительным свойством: среди тысяч разнообразных белков они «узнают» только один белок - чужеродный и только с ним реагируют. Такой механизм сопротивления возбудителям заболеваний называют иммунитетом. Помимо антител, растворенных в крови, имеются антитела на поверхности специальных клеток, которые «узнают» и захватывают чужеродные клетки. Это клеточный иммунитет, обеспечивающий в большинстве случаев и уничтожение вновь возникающих раковых клеток.
Чтобы предупредить заболевание, людям и животным вводят ослабленные или убитые бактерии либо вирусы (вакцины), которые не вызывают болезнь, но заставляют специальные клетки организма производить антитела против этих возбудителей. Если через некоторое время болезнетворная неослабленная бактерия или вирус попадают в такой организм, они встречают прочный защитный барьер из антител. Миллионы человеческих жизней спасены вакцинацией против оспы, бешенства, полиомиелита, желтой лихорадки и других болезней.
Белки - источник энергии. Белки могут служить источником энергии для клетки. При недостатке углеводов или жиров окисляются молекулы аминокислот. Освободившаяся при этом энергия используется на поддержание процессов жизнедеятельности организма.

Основные типы биополимеров
Углеводы
Мономеры углеводов – простые сахара или моносахариды. Чаще всего это глюкоза и фруктоза. Самая важная функция моносахаридов – обеспечение организма энергией. В живых клетках простые сахара расщепляются до двуокиси углерода и воды, что сопровождается высвобождением энергии. Эту энергию клетки используют для своих разнообразных нужд.

Глюкоза – это базовая форма, которая хранится в человеческом организме, как запас энергии в виде гликогена в мышцах и печени. В природе глюкоза содержится в сладких фруктах и овощах: винограде, ягодах, апельсинах, моркови, кукурузе. Глюкоза также производится в промышленном масштабе. Пример – кукурузный сироп
Фруктоза содержится в меде, спелых сладких фруктах и овощах. Перед усвоением глюкозы, организм должен сначала конвертировать фруктозу в глюкозу.

Строение молекулы глюкозы Линейная форма глюкозы: СНОСН(ОН)СН(ОН)СН(ОН)СН(ОН)СН2(ОН)
Глюкоза преимущественно существует в циклическом виде. Известны a- и b-формы циклической глюкозы, различающиеся ориентацией гидроксила при С-1:

Простые сахара могут соединяться друг с другом, образуя дисахариды
Сахароза – столовый сахар, получаемый из сахарной свеклы, тростника, а также коричневый сахар, черная патока. Содержится в небольшом количестве в овощах и фруктах.
Лактоза – молочный сахар, единственный углевод животного происхождения, поэтому очень важный в питании человека. Содержание лактозы в молоке зависит от вида молока и варьируется от 2 до 8%.
Мальтоза - солодовый сахар, формируется в процессе образования солода и ферментации винограда. Присутствует в пиве, мюслях и детском питании, обогащенных мальтозой.

Липиды
Липиды разнообразны по структуре и по соотношению входящих в них элементов. Однако все они имеют общее свойство – все они неполярны. Они растворяются в хлороформе и эфирах, но практически нерастворимы в воде. Благодаря этому свойству липиды являются важнейшими компонентами мембран.
Липиды –главная форма хранения энергии в животном организме, хранятся в концентрированном виде (без воды). Любое избыточное количество сахара, не израсходованное сразу, быстро превращается в жир. Существует три группы липидов:

Триглицеролы (или триглицериды) – это молекулы, образованные в результате присоединения трех остатков жирных кислот к одной молекуле трехатомного спирта глицерола.
В этой группе различают жиры и масла. Жиры при комнатной температуре остаются твердыми, а масла сохраняют жидкую консистенцию. В маслах содержится больше ненасыщенных жирных кислот.

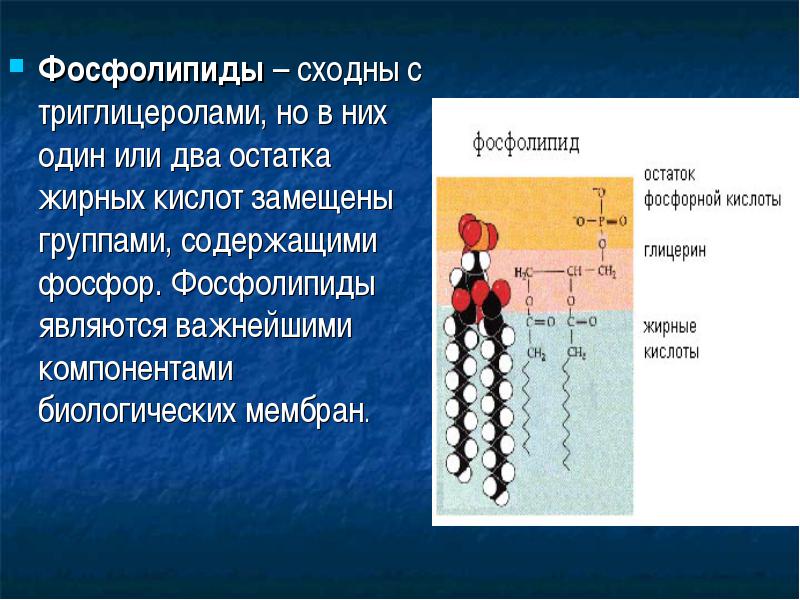
Фосфолипиды – сходны с триглицеролами, но в них один или два остатка жирных кислот замещены группами, содержащими фосфор. Фосфолипиды являются важнейшими компонентами биологических мембран.
Стероиды – это липиды, в основе которых лежит основа из четырех колец. У различных стероидов к этому основному скелету присоединяются боковые группы. К стероидам относится ряд гормонов (половые гормоны, кортизон). Стероид холестерол – важный компонент клеточных мембран у животных, но его избыток в организме может привести к образованию желчных камней и к заболеваниям сердечно-сосудистой системы.
Строение молекулы холестерола

Белки
В состав белка входят углерод, кислород, водород и азот. Некоторые белки содержат еще и серу. Роль мономеров в белках играют аминокислоты.
У каждой аминокислоты имеется карбоксильная группа (-СООН) и аминогруппа (-NH2).
В белках встречаются 20 обычных видов аминокислот.
Функции белков – ферментативная, строительная (мембраны), энергетическая, двигательная, защитная и регуляторная.

Для белков характерны четыре структуры:
Первичная – полипептид, длинная цепь, содержащая от 100 до 300 аминокислот, образуется за счет пептидных связей.

Вторичная – образуется в результате формирования водородных связей между соседними пептидными связями. При формировании вторичной структуры молекула белка упаковывается либо в левозакрученную спираль, либо в бета-конфигурацию, характерную для белков, выполняющих строительную функцию.


Третичная формируется в результате образования 4-х видов связей: водородных, ионных взаимодействий, образования дисульфидных мостиков и гидрофильно-гидрофобных связей (Ван-Дер-Валя).
Существует глобулярная и фибрилярная третичные структуры. Третичная структура для большинства белков является рабочей, т.к. она энеогетически более выгодна.

Некоторые белки формируют четвертичную структуру – она представляет собой комплексы белков и других органических веществ. Формирующие силы такие же как и у третичной структуры.
Денатурация белка
Это потеря биологической активности белков при разрыве слабых связей, разрушение нативной (природной) структуры белка под действием денатурирующих агентов: высокой температуры, УФО, кислот, щелочей, ионов тяжелых металлов. Денатурация бывает обратимая (ренатурация) и необратимая.



